Aperçu des sections
- Généralités
- Chap I STEREOCHIMIE
Chap I STEREOCHIMIE
STEREOCHIMIE
1- 1- Rappel : Structure géométrique
Structure tétraédrique des alcanes
Structure plane de la double liaison
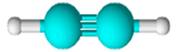
Structure linéaire de la triple liaison



 méthane CH4
méthane CH4
éthylène CH2= CH2

acétylène
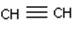
2- 2- isomérie
Deux molécules sont isomères si elles ont la même formule brute mais sont différentes par l’arrangement ou bien la disposition des atomes dans l’espace
a) a) isomère de constitution
Deux isomères de constitution ont même formule brute mais possèdent des formules semi-développées différentes
· - Isomère de chaîne : butane et 2-méthylpropane
Différents par l’enchainement des carbones
· - Isomère de position : but-1-ène et but-2-ène,
propan-1-ol et propan-2-ol
La position des groupes fonctionnels ou bien des liaisons multiples change
· - Isomère de fonction : groupes fonctionnels différents pour une même formule brute
Alcool et éther-oxyde CnH2n+2O
Cétone et aldéhyde CnH2nO
Acide carboxylique et ester CnH2nO2
b) b) Stéréoisomérie
Deux stéréo-isomères ont la même formule semi-développée mais elles n’ont pas les mêmes structures spatiales (elles ne sont pas superposables)
· - Isomère de conformation : une conformation donnée est obtenue par rotation de la molécule autour d’une liaison simple C - C
Exemple : éthane



 Conformation éclipsée
Conformation éclipsée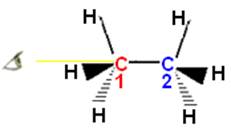
Représentation de NEWMAN
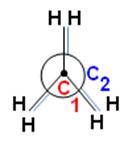
Conformation étoilée ou décalée
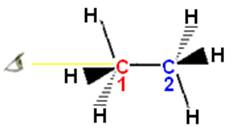
Représentation de NEWMAN

Remarque :
Il y a une forte répulsion entre les atomes pour la conformation éclipsée : l’énergie de la molécule est maximale d’où son instabilité. Pour la conformation étoilée ou décalée, la répulsion entre les atomes est minimale, l’énergie de la molécule est minimale : c’est la forme la plus stable. La forme éclipsée ou décalée ne peut être isolée.
· - Isomère de configuration : le passage d’une configuration à une autre nécessite la rupture d’une liaison
Exemple 1 : isomérie Z/E concernant les alcènes de types R – CH – CH – R’
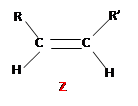
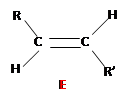
Exemple 2: énantiomère
Le carbone asymétrique C* est un carbone tétragonal lié à 4 groupes d’atomes différents.
butan-2-ol :CH3 – CHOH – CH2 – CH3
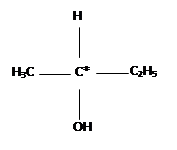
Les deux énantiomères sont images l’une de l’autre par un miroir plan, elles ne sont pas superposables et possèdent les mêmes propriétés physiques à part leur activité optique.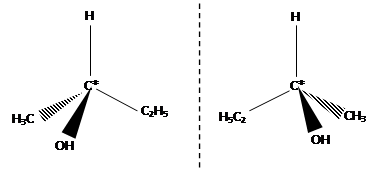
- Chiralité : c’est la propriété d’un objet de ne pas être superposable à son image donné par un miroir plan. Une molécule ou ion contenant un seul carbone asymétrique est chirale.
- Activité optique : Une solution contenant un des énantiomères« dextrogyre » est traversée par un faisceau provoque la rotation du plan de polarisation vers la droite. L’autre énantiomère « lévogyre » produit l’effet inverse (rotation du plan de polarisation vers la gauche
- Un mélange racémique est un mélange équimolaire des deux énantiomères, un tel mélange est optiquement inactif.
Mr RANDRIANANTENAINA Chabanas Deloy
email: chabanasdeloy@gmail.com
